上海金畔生物科技有限公司代理AAT Bioquest荧光染料全线产品,欢迎访问AAT Bioquest荧光染料官网了解更多信息。
Cell Meter 线粒体膜电位检测试剂盒 红色荧光 适合微孔板检测
 |
货号 | 22807 | 存储条件 | 在零下15度以下保存, 避免光照 |
| 规格 | 500 tests | 价格 | 2544 | |
| Ex (nm) | 613 | Em (nm) | 631 | |
| 分子量 | 溶剂 | |||
| 产品详细介绍 | ||||
简要概述
我们的Cell Meter 检测试剂盒是一套用于检测细胞生存力的工具。可以使用多种参数。该特定试剂盒旨在通过测量线粒体膜电位(MMP)的消失来检测细胞凋亡。 MMP的凋亡与线粒体通透性过渡孔的开放相吻合,导致细胞色素C释放到细胞质中,进而触发了细胞凋亡级联反应中的其他下游事件。我们的Cell Meter 线粒体膜电位测定试剂盒可通过优化的测定方法提供所有基本成分。荧光测定法使用我们专有的阳离子MitoTell Red检测MMP消失的细胞凋亡。在正常细胞中,当MitoTell Red堆积在线粒体中时,红色荧光强度会增加。但是,在凋亡细胞中,MMP凋亡后,MitoTell Red的荧光强度降低。 MitoTell Red染色的细胞可以通过荧光显微镜Cy5通道或荧光酶标仪读取。该试剂盒经过优化,可通过荧光酶标仪读取凋亡激活剂和抑制剂。而且该测定可以以方便的96孔和384孔荧光酶标仪进行检测,而无需清洗步骤。金畔生物是AAT Bioquest的中国代理商,为您提供最优质的Cell Meter 线粒体膜电位检测试剂盒。
适用仪器
| 荧光酶标仪 | |
| 激发: | 610nm |
| 发射: | 650nm |
| cutoff: | 630nm |
| 推荐孔板: | 黑色透明 |
| 读取模式: | 底读模式 |
产品说明书
样品实验方案
简要概述
- 准备细胞
- 添加测试化合物
- 添加MitoTell Red工作溶液(100 µL /孔/ 96孔板或25 µL /孔/ 384孔板)
- 将板在5%CO2、37°C的培养箱中孵育30分钟
- 添加测定缓冲液B(50 µL /孔/ 96孔板或12.5 µL /孔/ 384孔板)
- 在Ex / Em = 610/650 nm(截止= 630 nm)或使用Cy5滤光片的荧光显微镜下检测荧光增加(底部读取模式)
溶液配制
将50 µL的200X MitoTell Red(组分A)添加到10 mL的测定缓冲液A(组分B)中,并充分混合以制成MitoTell Red工作溶液,避光。
实验步骤
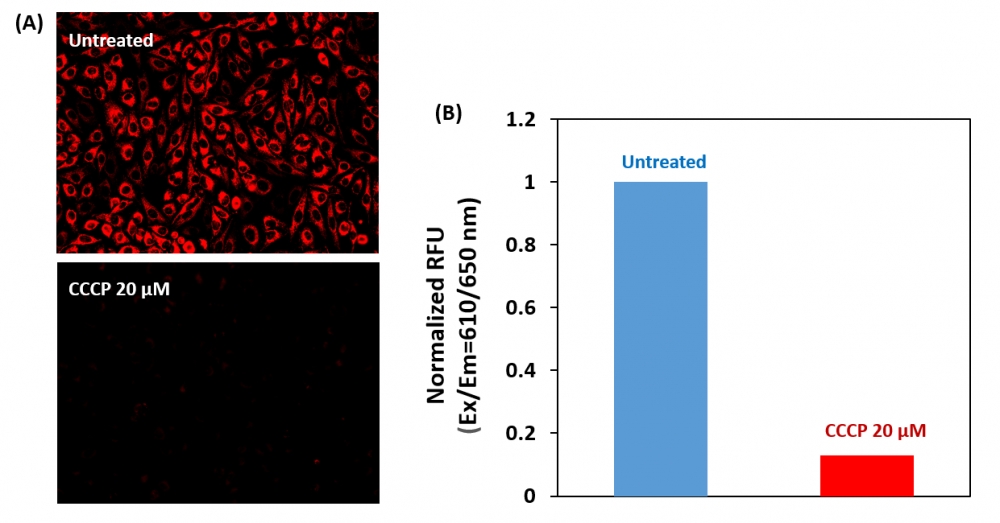
1.用测试化合物处理细胞一段时间,以诱导细胞凋亡,并建立平行对照实验。注意:我们用20 µM CCCP处理HeLa细胞15分钟,以改变线粒体膜电位。CCCP或FCCP可以与MitoTell Red同时添加。为了获得最佳结果,可能需要为每个单独的细胞系滴定CCCP或FCCP。
2.将100 µL /孔/ 96孔板或25 µL /孔/ 384孔板的MitoTell Red工作溶液加入细胞板。
3.在避光的条件下,将板在37ºC下孵育15-30分钟。注意:适当的孵育时间取决于所用的单个细胞类型和细胞浓度。优化每个实验的孵育时间。
4.将50 µL /孔/ 96孔板或12.5 µL /孔/ 384孔板的测定缓冲液B(组分C)添加到细胞板中。注意:加载后请勿洗涤细胞。对于非贴壁细胞,建议在加入测定缓冲液B(组分C)后,以800 rpm离心细胞板2分钟,然后制动。
5.加入测定缓冲液B(组分C)后10到30分钟,用荧光酶标仪(Ext / Em = 610/650 nm(截止= 630 nm))检测荧光强度,或在荧光下用带Cy5滤镜的显微镜观察荧光信号。
参考文献
Safranine O as a fluorescent probe for mitochondrial membrane potential studied on the single particle level and in suspension
Authors: Perevoshchikova IV, Sorochkina AI, Zorov DB, Antonenko YN.
Journal: Biochemistry (Mosc) (2009): 663
Computer-assisted live cell analysis of mitochondrial membrane potential, morphology and calcium handling
Authors: Koopman WJ, Distelmaier F, Esseling JJ, Smeitink JA, Willems PH.
Journal: Methods (2008): 304
Determination of high mitochondrial membrane potential in spermatozoa loaded with the mitochondrial probe 5,5′,6,6′-tetrachloro-1,1′,3,3′-tetraethylbenzimidazolyl-carbocyanine iodide (JC-1) by using fluorescence-activated flow cytometry
Authors: Guthrie HD, Welch GR.
Journal: Methods Mol Biol (2008): 89
Effects of eprosartan on mitochondrial membrane potential and H2O2 levels in leucocytes in hypertension
Authors: Labios M, Martinez M, Gabriel F, Guiral V, Ruiz-Aja S, Beltran B, Munoz A.
Journal: J Hum Hypertens (2008): 493
Evaluation of sperm mitochondrial membrane potential by JC-1 fluorescent staining and flow cytometry
Authors: Xia XY, Wu YM, Hou BS, Yang B, Pan LJ, Shi YC, Jin BF, Shao Y, Cui YX, Huang YF.
Journal: Zhonghua Nan Ke Xue (2008): 135
How DASPMI reveals mitochondrial membrane potential: fluorescence decay kinetics and steady-state anisotropy in living cells
Authors: Ramadass R, Bereiter-Hahn J.
Journal: Biophys J (2008): 4068
Life cell quantification of mitochondrial membrane potential at the single organelle level
Authors: Distelmaier F, Koopman WJ, Testa ER, de Jong AS, Swarts HG, Mayatepek E, Smeitink JA, Willems PH.
Journal: Cytometry A (2008): 129
Mitochondrial membrane potential in axons increases with local nerve growth factor or semaphorin signaling
Authors: Verburg J, Hollenbeck PJ.
Journal: J Neurosci (2008): 8306
The mitochondrial membrane potential and Ca2+ oscillations in smooth muscle
Authors: Chalmers S, McCarron JG.
Journal: J Cell Sci (2008): 75
Cyclosporin A-induced oxidative stress is not the consequence of an increase in mitochondrial membrane potential
Authors: van der Toorn M, Kauffman HF, van der Deen M, Slebos DJ, Koeter GH, Gans RO, Bakker SJ.
Journal: Febs J (2007): 3003
